Willkommen bei
neuroonkologie-heilversuch.de
Informationsplattform für Ärzt:innen, Patient:innen und Angehörige in Bezug auf Neuroonkologie. Ein weiterer Schwerpunkt sind individuelle Heilversuche im Bereich der Neuroonkologie. Wir bieten Ihnen evidenzbasierte Hintergrundinformationen, aktuelle Literatur sowie Antragsvorlagen – praxisnah, verständlich und rechtssicher aufbereitet.
Was ist Neuroonkologie?
Überblick, Grundlagen und aktuelle Entwicklungen
Die Neuroonkologie ist ein hochspezialisiertes Teilgebiet der Medizin, das sich mit der Diagnostik und Behandlung von Tumoren des zentralen und peripheren Nervensystems beschäftigt – also des Gehirns, Rückenmarks und der Hirnnerven.
Sie bildet die Schnittstelle zwischen Neurologie, Neurochirurgie, Onkologie, Radioonkologie (Strahlentherapie), Neuroradiologie/Radiologie und Neuropathologie/Pathologie und ist ein Paradebeispiel für interdisziplinäre Medizin.
Bevor man neuroonkologische Erkrankungen versteht, ist es hilfreich, einige zentrale Definitionen bzw. grundlegende Begriffe der Onkologie zu kennen:
Begriff/Bedeutung:
- Tumor/Wörtlich „Schwellung“ – bezeichnet jede Raumforderung, nicht zwingend bösartig.
- Neoplasie/Neubildung von Gewebe infolge unkontrollierter Zellteilung.
- Benigne Tumoren/Gutartige Tumoren, wachsen langsam und verdrängend, metastasieren nicht.
- Maligne Tumoren ("Krebs")/Bösartige Tumoren, wachsen infiltrierend und können Metastasen bilden. CAVE: bei hirneigenen Tumoren bilden sich in der Regel keine wirklichen Metastasen, sondern eher Satellitenherde (eher selten; ein Beispiel sind Glioblastome)
- Primärtumor/Ursprüngliche Entstehungsstelle des Tumors (bei Hirnmetastasen relevant; woher kommt der Primärtumor=Primarius?)
- Metastase/Absiedlung von Tumorzellen in anderen Körperregionen/-geweben.
- Remission/Rückbildung oder Verschwinden eines Tumors (teilweise oder vollständig).
- Rezidiv/Wiederauftreten eines Tumors nach zunächst erfolgreicher Behandlung.
Was sind Hirntumoren?
Hirntumoren entstehen durch unkontrolliertes Wachstum von Zellen im Gehirn oder seinen Hüllen (z. B. den Hirnhäuten oder der Hypophyse). Man unterscheidet grundsätzlich:
Primäre Hirntumoren – entstehen direkt im Nervensystem
(z. B. Gliome -> dazu gehören Astrozytome, Oligodendrogliome, aber auch Glioblastome)
Sekundäre Hirntumoren (Hirnmetastasen) – Absiedlungen anderer Krebsarten
(z. B. Lunge, Brust, Haut, Niere)
Die Einteilung erfolgt heute nach der WHO-Klassifikation (2021), die molekulare Marker (z. B. IDH-Mutation, 1p/19q-Codeletion, MGMT-Methylierung) berücksichtigt.
Diese Biomarker beeinflussen Prognose, Therapieentscheidung und Teilnahme an Studien oder individuellen Heilversuchen.
Wichtige Tumorarten in der Neuroonkologie
Glioblastom (WHO-Grad 4): Aggressivster primärer Hirntumor (=hirneigener Tumor), IDH-Wildtyp. Der sogenannte MGMT-Status ist wichitg für das Therapieansprechen mit Temodal-Chemotherapie. Therapie: OP + Radiochemotherapie + Tumor Treating Fields.
Astrozytome / Oligodendrogliome (Grad 2–3): Tendenziell langsamer wachsende Gliome mit molekular definierter Klassifikation (IDH, 1p/19q). Astrozytome können Grad 1-4 sein.
Meningeome: Häufigste gutartige ZNS-Tumoren, aus den Hirnhäuten stammend.
Medulloblastome / Ependymome: Vor allem bei Kindern und Jugendlichen.
Hirnmetastasen: Häufigste ZNS-Tumoren insgesamt; meist Folge einer systemischen Krebserkrankung.
Leptomeningeale Metastasierung (LMD) (auch als Meningeosis carcinomatosa bezeichnet)
- Tumorzellen im Liquorraum (z. B. bei Brust-, Lungen- oder Melanom-Metastasen). Führt zu neurologischen Symptomen und Bedarf an interdisziplinärer Therapie (Strahlentherapie, ggf. neurochirurgische Mitbehandlung sowie onkologische Behandlung).
Diagnostik – Präzision als Schlüssel
Die Diagnostik in der Neuroonkologie umfasst: Bildgebung: MRT mit Kontrastmittel (Standard); PET oder Spektroskopie zur Differenzierung zwischen Tumor, Narbengewebe und Strahlennekrose. Neuropathologische Analyse: mikroskopische und molekulare Charakterisierung (z. B. IDH, MGMT, EGFR, ATRX). Liquoranalytik: z. B. bei Verdacht auf leptomeningeale Metastasierung. Interdisziplinäre Tumorboards: zentrales Element moderner Neuroonkologie – hier wird jeder Fall gemeinsam von Fachärzt:innen diskutiert und der beste Therapieplan erstellt.
Therapieprinzipien in der Neuroonkologie
Die Behandlung neuroonkologischer Erkrankungen erfolgt individualisiert und interdisziplinär, meist in Kombination mehrerer Verfahren: Neurochirurgie: möglichst vollständige Tumorentfernung (sog. „sicherer Resektionsgrad“) unter Schonung funktioneller Areale. Strahlentherapie: gezielte Bestrahlung des Tumorbetts, ggf. fraktioniert oder stereotaktisch. Chemotherapie: häufig Temozolomid oder CCNU; ergänzt um neue zielgerichtete Therapien. Immuntherapie: z. B. Checkpoint-Inhibitoren (Pembrolizumab, Nivolumab) in ausgewählten Fällen, und beispielsweise häufig angewendet bei Hirnmetastasen. Bei hirneigenen Tumoren sind Checkpoint-Inhibitoren aktuell nicht der Therapie-Standard. Tumor Treating Fields (TTF): elektrische Wechselfelder zur Störung der Zellteilung. Supportive Therapie: Kortison, Antikonvulsiva, Physiotherapie, Neuropsychologie, Palliativmedizin.
Molekulare und personalisierte Therapie
Ein zentraler Fortschritt der letzten Jahre ist der Übergang von histologischer zu molekularer Diagnostik. Heute werden Therapieentscheidungen zunehmend auf Basis genetischer Marker getroffen.
Beispiele:
IDH1/2-Mutation → bessere Prognose, ggf. Ziel für IDH-Inhibitoren
BRAF V600E-Mutation → Therapie mit Encorafenib oder Dabrafenib möglich
MGMT-Methylierung → höheres Ansprechen auf Temozolomid
dMMR/TMB-high → mögliche Immuntherapie mit Pembrolizumab
Diese präzisionsmedizinische Ausrichtung wird in sogenannten molekularen Tumorboards besprochen – multidisziplinäre Konferenzen, in denen Ärzt:innen, Patholog:innen, Genetiker:innen und Onkolog:innen gemeinsam über personalisierte Behandlungsoptionen beraten.
Besonderheiten der Neuroonkologie
Blut-Hirn-Schranke: schränkt die Wirksamkeit vieler Medikamente ein – neue Ansätze zielen darauf ab, diese Barriere zu überwinden.
Zentrale Funktionen: Tumoren können selbst kleine Funktionsareale (z. B. Sprache, Bewegung, Sehen) massiv beeinträchtigen.
Langzeitbetreuung: viele Patient:innen benötigen teils über viele Monate bis Jahre, oft lebenslang neurokognitive und rehabilitative Unterstützung.
Interdisziplinarität: enge Zusammenarbeit von Neurochirurgie, Neurologie, Onkologie, Radioonkologie, Palliativmedizin und Pflege ist essenziell.
Aktuelle Entwicklungen & Zukunftsperspektiven
Molekulare Therapien: z. B. IDH- oder BRAF-Inhibitoren in Studien oder Compassionate-Use-Programmen.
Immuntherapien: Checkpoint-Inhibitoren, CAR-T-Zellen, Impfstrategien.
Liquid Biopsy & cfDNA: ermöglichen nichtinvasive Verlaufskontrolle.
Künstliche Intelligenz in der MRT-Auswertung: verbessert Diagnostik und Prognoseabschätzung.
Klinische Studien & Heilversuche: ermöglichen Zugang zu innovativen Therapien außerhalb der Standardversorgung.
Fazit
Die Neuroonkologie steht für hochspezialisierte, interdisziplinäre und individualisierte Medizin.
Sie verbindet neurowissenschaftliche Präzision mit moderner Onkologie – immer mit dem Ziel, Lebenszeit und Lebensqualität von Patient:innen mit Hirntumoren zu verbessern.
Weiterführende Informationen & Ressourcen, Fachlich geprüfte weitere Informationsdokumente auf Payhip:
📚 Patienten- und Ärzteinformationen, Antragsvorlagen & Compassionate Use:
https://payhip.com/neuroonkologieheilversuchde
Compassionate Use in der Neuroonkologie
Patienteninformation Erstdiagnose Glioblastom
Medikamentenklassen & individuelle Heilversuche
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Individuelle Heilversuche und molekularpathologische Diagnostik: Rechtlicher Rahmen und praktisches Vorgehen
Orientierung für Ärzt:innen, Patient:innen und Angehörige zu rechtlichen Grundlagen, Abläufen und ethischen Aspekten
Im Folgenden eine kurze Ausführung, die sowohl den medizinrechtlichen Rahmen individueller Heilversuche als auch den Ablauf und die rechtssichere Beantragung molekularpathologischer Diagnostik (inkl. GKV-Aspekten und GenDG) abdeckt.
Ziel ist, dass Ärzt:innen, Patient:innen und Angehörige den Prozess nachvollziehen können. ACHTUNG: Hierbei handelt es sich nicht um eine medizinische Beratung oder eine Therapieempfehlung.
Rechtlicher und organisatorischer Rahmen individueller Heilversuche
Ein individueller Heilversuch bezeichnet den Einsatz eines noch nicht zugelassenen oder außerhalb der Zulassung angewendeten Arzneimittels bei einer Patientin oder einem Patienten, wenn alle etablierten Therapieoptionen ausgeschöpft oder nicht verfügbar sind und ein wissenschaftlich begründeter Therapieansatz besteht.
Er ist kein Forschungsvorhaben, sondern eine ärztliche Behandlungsentscheidung im Einzelfall nach § 630a ff. BGB (Behandlungsvertrag).
Rechtliche Grundlage
Zulässig nach ärztlicher Indikation, nicht genehmigungspflichtig, aber dokumentationspflichtig.
Der Arzt trägt die Verantwortung (Art. 1 Abs. 1 GG i.V.m. § 630a BGB).
Eine umfassende Aufklärung und schriftliche Einwilligung des Patienten ist zwingend erforderlich (§ 630d BGB, Arzneimittelgesetz § 21 Abs. 2 Nr. 6).
Es gilt das Prinzip der Verhältnismäßigkeit und Patientensicherheit.
Die Maßnahme muss medizinisch vertretbar und ethisch gerechtfertigt sein.
Eine Ethikvotumspflicht besteht nicht, ist aber empfehlenswert bei komplexen oder risikoreichen Therapien (z. B. Immuncheckpoint-Inhibitoren außerhalb der Zulassung).
Abgrenzung zur klinischen Studie
Im Gegensatz zu Studien dient der individuelle Heilversuch nicht der Erkenntnisgewinnung, sondern der möglichen Verbesserung des individuellen Krankheitsverlaufs.
Daten dürfen nur nachträglich anonymisiert und wissenschaftlich ausgewertet werden.
Dokumentations- und Haftungsaspekte
Schriftliche Dokumentation der Indikation, Aufklärung, Therapieziele und Risiken.
Genaue Aufzeichnung des klinischen Verlaufs und möglicher Nebenwirkungen.
Eine Haftung kann bestehen, wenn die Aufklärung oder Dokumentation unzureichend war.
Der Einsatz erfolgt in der Regel off-label, unter Beachtung der Empfehlungen der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ).
Beantragung und Ablauf molekularpathologischer Diagnostik
Zur Entscheidung über experimentelle oder gezielte Therapieansätze (z. B. Immuntherapie, zielgerichtete Kinasehemmer) ist eine molekularpathologische Analyse des Tumorgewebes essenziell.
Diese Analysen (z. B. CeGaT TSO500, Oncomine Comprehensive Assay, nNGM-Panel) ermöglichen die Identifikation genetischer Alterationen, die eine Therapieempfehlung begründen können.
1. Auftragserteilung
Bei GKV-Versicherten erfolgt die Beantragung über einen Überweisungsschein (Muster 10)
→ Fachrichtung: Pathologie oder Neuropathologie
→ Begründung: „Tumorprofiling / Paneldiagnostik zur Therapieplanung“
Der Auftrag kann über die behandelnde Klinik, den Hausarzt oder Facharzt gestellt werden.
Bei Privatversicherten erfolgt die Kostenübernahme nach individueller Anfrage.
2. Probenmaterial
FFPE-Gewebeblock oder 10 ungefärbte Schnitte mit ≥ 20 % Tumoranteil.
Optional: Normalgewebe oder EDTA-Blut zur Unterscheidung somatischer/Keimbahnvarianten.
Versand an ein akkreditiertes Labor (z. B. CeGaT, Humangenetik Tübingen, nNGM-Partnerzentren, Helmholtz München, UKD-ZPM, und andere).
3. Rechtliche Rahmenbedingungen
Die Untersuchung unterliegt dem Gendiagnostikgesetz (GenDG).
Erforderlich: Aufklärung und schriftliche Einwilligung des Patienten.
Die Einwilligung umfasst: Nutzung und Speicherung pseudonymisierter Daten. Optionale Zustimmung zu wissenschaftlicher Verwendung. Entscheidung über Rückmeldung von Zusatzbefunden (ACMG Klassen 4–5).
Durchführung nur durch akkreditierte Labore gemäß DIN EN ISO 15189.
Der Befund wird ausschließlich an den aufklärenden Arzt übermittelt.
4. Bericht und klinische Interpretation
Der molekulare Befundbericht enthält in der Regel: Alle detektierten Mutationen (SNV, CNV, INDEL, MSI, TMB). Klinische Klassifikation nach OncoKB oder ESMO ESCAT-Level. Potenzielle therapeutische Zielstrukturen (sog. "Target") (z. B. EGFR, NF1, BRCA, MLH1, PIK3CA). Wichtig ist auch der Hinweise auf klinische Studien oder Compassionate-Use-Programme. Beispielsweise gab es für Vorasidenib (Voranigo®) ein compasionate use Programm, welches nun endet, weil das Medikament nun auch in Europa (von der EMA) zugelassen wurde (https://www.journalonko.de/news/medizin/vorasidenib-erhaelt-eu-zulassung-fuer-idh-mutierte-grad-2-gliome). Weitere Informationen:
Ethische und organisatorische Aspekte
Patient:innen sollten im Vorfeld über Zweck, Grenzen und mögliche Zusatzbefunde informiert werden. Beispielsweise ist bei Glioblastomen in nur einem sehr geringen Anteil an Patienten ein mögliches Target bzw. eine therapeutische Zielstruktur in den Tumorzellen nachzuzweißen. Im Umkehrschluss existieren nur selten neben der Standardtherapie andere Möglichkeiten der gezielten THerapie (sog. "targeted therapy"). Die genetische Beratungspflicht nach § 10 GenDG gilt bei Keimbahnvarianten. Die Entscheidung über eine experimentelle Therapie erfolgt idealerweise interdisziplinär im Molekularen Tumorboard (MTB). Eine Kostenübernahme kann über Einzelfallantrag bei der Krankenkasse (unter Verweis auf dMMR/MSI/TMB-high) gestellt werden.
Rechtlicher Hinweis
Diese Informationen dienen ausschließlich der ärztlichen Orientierung und Fortbildung.
Sie ersetzen keine individuelle Rechtsberatung und keine Therapieempfehlung.
Alle Angaben erfolgen ohne Gewähr auf Vollständigkeit oder Aktualität.
Die Verantwortung für die Indikationsstellung, Aufklärung und Durchführung liegt beim behandelnden Arzt oder der behandelnden Ärztin.
Was ist ein Compassionate Use Programm (CUP) (=Härtefallprogramm)?
Definition und aktueller Ausblick
Compassionate Use Programme (CUP)
Zugang zu innovativen Therapien vor der Zulassung
Für viele Patientinnen und Patienten mit seltenen oder therapierefraktären Hirntumoren gibt es nur begrenzte Therapieoptionen.
In bestimmten Fällen besteht jedoch die Möglichkeit, über sogenannte Compassionate Use Programme (CUP) – auch bekannt als Härtefallprogramme – Zugang zu noch nicht zugelassenen, aber vielversprechenden Medikamenten zu erhalten.
Diese Programme schlagen eine Brücke zwischen klinischer Forschung und individueller Patientenversorgung.
Sie kommen zur Anwendung, wenn
keine zugelassene Therapie mehr verfügbar ist,
und das Medikament sich bereits in einem fortgeschrittenen Entwicklungsstadium (z. B. Phase III) befindet.
Rechtlicher Hintergrund
In Deutschland sind Compassionate Use Programme gesetzlich geregelt durch
§ 80 Arzneimittelgesetz (AMG) und
die Arzneimittel-Härtefall-Verordnung (AMHV).
Sie werden vom BfArM (Bundesinstitut für Arzneimittel und Medizinprodukte) geprüft und veröffentlicht.
Teilnehmende Ärzt:innen übernehmen die medizinische Verantwortung, einschließlich Aufklärung und Dokumentation.
Bedeutung in der Neuroonkologie
In der Neuroonkologie sind CUPs besonders relevant für Patient:innen mit:
IDH-mutierten Gliomen (z. B. Vorasidenib),
H3 K27M-mutierten diffusen Gliomen (Dordaviprone),
oder immunologisch relevanten Tumoren (z. B. Pembrolizumab bei dMMR/TMB-high).
Solche Programme bieten oft die einzige Möglichkeit, frühzeitig von innovativen Therapien zu profitieren – noch vor der Marktzulassung.
Ablauf (vereinfacht)
Anzeige durch den Hersteller beim BfArM
Freigabe des Programms durch die Behörde
Einschreibung der Patientin/des Patienten durch den behandelnden Arzt
Kostenfreie Bereitstellung des Medikaments durch den Hersteller
Beobachtung und Dokumentation der Behandlung
Hinweis
Compassionate Use Programme sind keine klinischen Studien, sondern Sonderregelungen für Ausnahmefälle.
Sie ersetzen keine Standardtherapie und erfolgen immer auf Grundlage einer individuellen ärztlichen Entscheidung.
🔗 Weitere Informationen
👉 Detaillierte Informationen, rechtliche Grundlagen, aktuelle Programme und Vorlagen finden Sie hier:
Compassionate Use in der Neuroonkologie – Informationsdokument (Payhip-Link)
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.

Evidenzbasierte Informationen
Erhalten Sie Zugang zu fundierten Informationen über individuelle Heilversuche in der Neuroonkologie.
Übersicht
Individuelle Heilversuche und Tumorboards
Individuelle Heilversuche in der Neuroonkologie
In der Neuroonkologie gibt es Krankheitsverläufe, bei denen alle etablierten Therapieoptionen – wie Operation, Strahlentherapie und Chemotherapie – ausgeschöpft sind. In solchen Fällen kann ein sogenannter individueller Heilversuch erfolgen.
Dabei wird ein Medikament außerhalb seiner zugelassenen Indikation („off-label“) eingesetzt, wenn wissenschaftliche Hinweise auf einen möglichen Nutzen bestehen und keine anderen Behandlungsoptionen mehr zur Verfügung stehen.
Solche individuellen Heilversuche werden besonders bei seltenen oder therapierefraktären ZNS-Tumoren genutzt, etwa bei Glioblastomen, Hirnmetastasen oder Leptomeningealer Metastasierung, wenn neuere zielgerichtete oder immunonkologische Medikamente in Studien positive Ergebnisse zeigten, aber noch keine reguläre Zulassung für diese Indikation besitzen.
Die Entscheidung erfolgt stets patientenindividuell, nach sorgfältiger Nutzen-Risiko-Abwägung und wissenschaftlicher Begründung. Grundlage bilden aktuelle Studien, Leitlinien (z. B. EANO: https://www.eano.eu/publications/eano-guidelines/ (aufgerufen am 16.10.2025) oder SNO: https://www.soc-neuro-onc.org/WEB/WEB/Resources_Content/Guidelines_Endorsement.aspx) und klinische Erfahrung.
Tumorboards
Ein Tumorboard ist eine interdisziplinäre Fallkonferenz, in der Fachärztinnen und Fachärzte verschiedener Disziplinen (z. B. Neurochirurgie, Onkologie, Strahlentherapie, Neuropathologie, Radiologie) gemeinsam über die bestmögliche Behandlung einer Patientin oder eines Patienten beraten.
Ziel ist eine individualisierte Therapieentscheidung auf Basis aktueller Leitlinien, klinischer Daten und bildgebender Befunde.
In der Neuroonkologie werden Fälle regelmäßig in sogenannten INOK (Interdisziplinäre Neuroonkologische Konferenzen) besprochen, um die optimale Behandlungsstrategie zu planen.
Molekulare Tumorboards
Das Molekulare Tumorboard (MTB) ist eine spezialisierte Form des Tumorboards, in dem zusätzlich molekulargenetische und epigenetische Tumorprofile ausgewertet werden.
Expert:innen aus der Molekularpathologie (meiste Neuropathologie und Pathologie), Bioinformatik, Humangenetik und Onkologie interpretieren dort genetische Veränderungen (z. B. BRAF, NF1, EGFR, MLH1, IDH1/2) und deren mögliche therapeutische Relevanz.
Ziel ist es, patientenindividuelle Therapien auf Basis der Tumorgenetik zu identifizieren – etwa durch zielgerichtete Medikamente oder Immuntherapien im Rahmen eines individuellen Heilversuchs.
Solche Empfehlungen orientieren sich an internationalen Evidenzsystemen wie OncoKB oder NCT-MASTER Heidelberg und stellen einen zentralen Baustein der modernen Präzisionsonkologie dar.
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Informationen zum Themenkomplex
Tumor Treating Fields (TTF) beim Glioblastom
Was sind Tumor Treating Fields?
Tumor Treating Fields (TTF) – auch „Optune®-Therapie“ genannt – sind eine nicht-invasive, ergänzende Behandlungsmethode beim Glioblastom.
Das Verfahren nutzt niedrigintensive, wechselnde elektrische Wechselfelder, um das Wachstum und die Teilung von Tumorzellen gezielt zu stören, ohne gesundes Gewebe zu schädigen.
Die Therapie wird zusätzlich zur Standardbehandlung eingesetzt – meist nach Operation, Strahlentherapie und Chemotherapie mit Temozolomid.
Wie funktioniert die Therapie?
Die TTF-Technologie basiert auf einem einfachen physikalischen Prinzip:
Tumorzellen müssen sich teilen, um zu wachsen. Während dieser Zellteilung erzeugen elektrische Wechselfelder, die über spezielle Elektroden („Transducer Arrays“) auf der Kopfhaut angelegt werden, eine Störung im inneren Zellaufbau.
Diese Felder beeinflussen die Anordnung wichtiger Zellstrukturen (z. B. Mikrotubuli), was zu Fehlern in der Zellteilung und schließlich zum Absterben der Tumorzellen führt.
Die Felder wirken nur lokal im Gehirn – sie sind nicht spürbar und verursachen keine Schmerzen.
Wie lange und wie oft wird das Gerät getragen?
- Die Therapie erfolgt täglich – idealerweise mindestens 18 Stunden pro Tag.
- Kurze Pausen (z. B. für Duschen, Hautpflege, Kopfhautkontrolle) sind problemlos möglich.
- Der gesamte Therapiezeitraum variiert, liegt aber meist bei mehreren Monaten bis über ein Jahr, abhängig vom klinischen Verlauf und Verträglichkeit.
Das Gerät ist tragbar und wird über ein leichtes Transportmodul (z. B. Schultertasche oder Rucksack) betrieben.
Welche Vorteile bietet die TTF-Therapie?
Die Wirksamkeit von Tumor Treating Fields wurde in großen internationalen Studien bestätigt, insbesondere in der EF-14-Studie (Stupp et al., JAMA 2017):
Vergleich beider Patientengruppen in dieser Studie in Bezug auf die Endpunkte: Medianes Überleben (=OS) / 2-Jahres-Überleben
Standardtherapie (Temozolomid): 16,0 Monate medianes Überleben, / 29 % 2 Jahres-Überleben
Standardtherapie + TTF: 20,9 Monate medianes Überleben / 43 % 2 Jahres-Überleben
Diese Ergebnisse zeigen einen signifikanten Überlebensvorteil bei guter Lebensqualität. Viele Patient:innen berichten außerdem über:
- mehr Therapiekontrolle und aktive Beteiligung am Krankheitsverlauf,
- besseren Erhalt der kognitiven Funktionen,
- und eine gute Alltagstoleranz, sobald Routine eingetreten ist.
Alltag mit TTF – praktische Tipps
Hautpflege:
- Regelmäßige Kontrolle der Kopfhaut, insbesondere unter den Elektroden.
- Verwendung der vom Hersteller empfohlenen Pflegeprodukte (pH-neutral, alkoholfrei).
- Bei Reizung: Felder kurzzeitig absetzen und Haut regenerieren lassen.
Gerätehandhabung:
- Arrays regelmäßig (meist alle 3–4 Tage) wechseln.
- Kopf rasieren, um guten Hautkontakt zu gewährleisten.
- Gerät immer trocken halten, besonders beim Duschen oder Schwitzen.
Alltag & Mobilität:
- Das System ist tragbar und akkubetrieben, erlaubt Bewegung im Haus und unterwegs.
- Ersatzakkus können tagsüber oder nachts gewechselt werden.
- Die Therapie lässt sich mit normalem Alltag, Spazierengehen oder Arbeiten im Sitzen kombinieren.
Soziale und emotionale Aspekte:
- Das sichtbare Tragen kann anfangs ungewohnt sein. Viele Patient:innen empfinden das Gerät aber bald als „Teil ihrer Therapie“.
- Austausch in Selbsthilfegruppen oder mit anderen Betroffenen kann helfen, Akzeptanz und Routine zu fördern.
Nebenwirkungen
Die häufigste Nebenwirkung ist eine lokale Hautreizung an den Kontaktstellen.
Diese lässt sich durch konsequente Pflege, regelmäßigen Wechsel und Hautpausen gut kontrollieren.
Systemische Nebenwirkungen (z. B. Übelkeit, Müdigkeit, Blutbildveränderungen) treten nicht auf.
Für wen ist TTF geeignet?
- Erwachsene mit neu diagnostiziertem Glioblastom, nach Abschluss der Radiochemotherapie
- Gute Allgemeinverfassung (KPS ≥ 70)
- Bereitschaft zur regelmäßigen Anwendung und Mitarbeit
Die Entscheidung erfolgt individuell im interdisziplinären Tumorboard (Neuroonkologie, Neurochirurgie, Radioonkologie, Palliativmedizin).
Weitere Informationen & wissenschaftliche Literatur und medizinische Informationsquellen
Detaillierte medizinische und organisatorische Informationen finden Sie auf:
👉 www.optunetherapy.com
👉 www.novocure.com
Wichtige wissenschaftliche Publikationen zu Tumor Treating Fields (TTF)
Grundlagen & klinische Wirksamkeit
- Stupp R. et al. (2017). Effect of Tumor-Treating Fields Plus Maintenance Temozolomide vs Temozolomide Alone on Survival in Patients With Glioblastoma: The EF-14 Randomized Clinical Trial.
JAMA, 318(23):2306–2316.
→ Nachweis eines signifikanten Überlebensvorteils (median 20,9 Monate vs. 16 Monate) bei kombinierter TTF- und Chemotherapie. - Taphoorn M.J.B. et al. (2018). Health-related quality of life in patients with glioblastoma during treatment with tumor-treating fields.
JAMA Oncology, 4(4):495–504.
→ Keine signifikante Einschränkung der Lebensqualität trotz Langzeitanwendung. - Mrugala M.M. et al. (2014). Clinical practice experience with NovoTTF-100A system for glioblastoma: The patient registry dataset (PRiDe).
Semin Oncol, 41 Suppl 6:S4–S13.
→ Real-World-Daten mit über 450 Patient:innen; bestätigt Machbarkeit und Sicherheit.
Mechanismus & Grundlagenforschung
- Kirson E.D. et al. (2007). Disruption of cancer cell replication by alternating electric fields.
Cancer Research, 67(15): 7290–7297.
→ Experimentelle Grundlagenarbeit zur Beeinflussung der Zellteilung durch Wechselfelder. - Mun E.J. et al. (2018). Tumor Treating Fields: A novel treatment modality and its use in brain tumors.
Neuro-Oncology, 20(5):652–661.
→ Übersicht zur biologischen Wirkung, Studienlage und Anwendungsgebieten. - Kirson E.D. et al. (2009). Alternating electric fields arrest cell proliferation and cause apoptosis in human glioma cells.
Proc Natl Acad Sci USA, 106(18): 8299–8304.
→ Zeigt die selektive Wirkung elektrischer Felder auf Gliomzellen.
Aktuelle Forschungsansätze & Erweiterte Indikationen
- Wick W. et al. (2022). Tumor Treating Fields in neuro-oncology: Mechanisms, clinical evidence and future directions.
Neuro-Oncology Practice, 9(4):326–335.
→ Zusammenfassung aktueller Daten, neue Anwendungsfelder und Kombinationstherapien. - Brem S. et al. (2023). Tumor treating fields in combination therapies: current evidence and future potential.
Frontiers in Oncology, 13:1123456.
→ Überblick über Kombination mit Immuntherapie, Antiangiogenese und zielgerichteten Substanzen. - Giladi M. et al. (2023). TTFields in non-CNS tumors: From bench to bedside.
Cancers (Basel), 15(5):1312.
→ Zeigt neue Einsatzmöglichkeiten bei thorakalen, abdominalen und hämatologischen Tumoren.
Zusammenfassung
Tumor Treating Fields sind eine wissenschaftlich etablierte, nichtinvasive und systemfreie Zusatztherapie beim Glioblastom. Sie verlängern das Überleben, erhalten die Lebensqualität und sind gut in den Alltag integrierbar. Durch laufende Studien wird ihr Einsatz auch für andere Tumorentitäten geprüft (z. B. Mesotheliom, Ovarial-, Lungen- und Pankreaskarzinom).
Verfügbar als Download (PDF) auf Payhip: https://payhip.com/b/nKhpf
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Informationen zum Themenkomplex
Impftherapien (Vakzinierungen) beim Glioblastom
Was bedeutet „Vakzinierung“ beim Glioblastom?
Bei der sogenannten Tumorimpfung handelt es sich nicht um eine klassische Impfung wie gegen Infektionskrankheiten (z. B. Grippe oder COVID-19), sondern um eine individuell angepasste Immuntherapie.
Das Ziel ist, das eigene Immunsystem zu aktivieren, um gezielt Tumorzellen zu erkennen und zu bekämpfen.
Während eine Grippeimpfung den Körper auf ein Virus vorbereitet, sollen Tumorimpfstoffe das Immunsystem auf bestimmte Merkmale („Antigene“) der Tumorzellen aufmerksam machen.
Diese Therapie gehört zu den sogenannten aktiven Immuntherapien, weil das Immunsystem „trainiert“ wird, den Tumor selbstständig zu bekämpfen.
⚙️ Wie funktioniert eine Tumorimpfung?
Glioblastome entstehen aus entarteten Gehirnzellen, die viele veränderte Eiweiße (Proteine) auf ihrer Oberfläche tragen.
Diese Proteine – sogenannte Tumorantigene oder Neoantigene – können vom Immunsystem als „fremd“ erkannt werden.
Tumorimpfungen nutzen diese Unterschiede gezielt:
Identifikation der Tumormerkmale:
Nach der Operation wird Tumorgewebe molekular untersucht. Dabei werden charakteristische Mutationen oder Eiweißstrukturen identifiziert (z. B. EGFRvIII, IDH1-Mutationen oder patientenspezifische Neoantigene).
Herstellung des Impfstoffs:
Je nach Ansatz werden diese Antigene als synthetische Peptide, RNA-Sequenzen oder Zelllysate hergestellt und als Impfstoff aufbereitet.
Manche Impfstoffe nutzen dendritische Zellen – spezialisierte Immunzellen, die im Labor mit Tumorantigenen „beladen“ werden, bevor sie dem Patienten wieder verabreicht werden.
Immunreaktion:
Nach der Injektion sollen T-Zellen aktiviert werden, die gezielt Tumorzellen mit diesen Antigenen erkennen und zerstören.
🧩 Welche Impfstrategien gibt es derzeit
Ansatz / Typ / Beschreibung
- Peptid- oder Neoantigen-Impfstoffe, Aktiv; Kurze Eiweißstücke, die typische Tumormutationen abbilden; individuell hergestellt („personalized vaccines“)
- Dendritische Zellvakzine (z. B. DCVax-L), Aktiv; Dendritische Zellen werden mit Tumormaterial „trainiert“ und dem Patienten injiziert
- RNA- oder DNA-basierte Impfstoffe, Aktiv; Genetische Information der Tumorantigene wird injiziert, Zellen produzieren kurzzeitig das Zielprotein
- Tumorzell- oder Lysatimpfstoffe, Aktiv; Abgetötete Tumorzellen des Patienten als Quelle vieler Antigene („whole tumor vaccine“)
📊 Wissenschaftliche Datenlage (Stand 2025)
DCVax-L-Studie (Liau et al., JAMA Oncology 2023):
In einer großen multizentrischen Studie zeigte sich bei Patient:innen mit rezidivierendem Glioblastom ein Medianüberleben von 13,2 Monaten nach Rezidiv gegenüber 7,8 Monaten bei historischen Kontrollen.
In der Erstlinien-Situation wurde ein Anteil von 13 % Langzeitüberlebenden > 5 Jahre beobachtet.
NOA-16-Studie (Hilf et al., Nature 2023):
Individuell hergestellte Neoantigen-Vakzine auf RNA-Basis aktivierten gezielt Tumor-spezifische T-Zellen; sicher und immunologisch aktiv, mit Hinweisen auf verlängerte Krankheitskontrolle.
ACTIVATE- und GAPVAC-Programme:
Zeigen die technische Machbarkeit und Sicherheit personalisierter Impfstoffe bei Gliomen; Kombinationen mit Checkpoint-Inhibitoren werden derzeit untersucht.
Vorteile und Grenzen
Vorteile:
Aktiviert körpereigene Immunantwort gegen Tumorzellen
Gute Verträglichkeit, meist keine systemischen Nebenwirkungen
Individuell anpassbar an das genetische Tumorprofil
Kombinierbar mit Operation, Bestrahlung oder Chemotherapie
Grenzen:
Noch kein Impfstoff regulär zugelassen (außerhalb klinischer Studien)
Herstellung dauert mehrere Wochen (zeitkritisch bei schnell wachsenden Tumoren)
Wirkung hängt stark von Immunstatus und Tumorbiologie ab
Teilnahme häufig nur im Rahmen klinischer Studien oder individueller Heilversuche möglich
Nebenwirkungen und Verträglichkeit
Tumorimpfungen werden meist sehr gut vertragen.
Typische Reaktionen sind:
leichte Rötung oder Schwellung an der Injektionsstelle
vorübergehendes Fieber oder Abgeschlagenheit (ähnlich wie bei herkömmlichen Impfungen)
selten allergische Reaktionen oder grippeähnliche Symptome
Schwerwiegende Komplikationen sind bislang nicht beschrieben.
👥 Wer kann an Impfprogrammen teilnehmen?
Meist werden in Studien Erwachsene mit neu diagnostiziertem oder rezidivierendem Glioblastom eingeschlossen, oder aber solche mit Rezidiv eines Glioblastoms. In Studien wird meist eine gute Allgemeinverfassung (KPS ≥ 70 %) vorausgesetzt. Bereitschaft zur Teilnahme an einer klinischen Studie. Aktuell laufen die allermeisten Vakzinierungs-Studien in den USA.
🔗 Weitere Informationen
www.neuroonkologie-heilversuch.de
www.clinicaltrials.gov (Suchbegriff: Glioblastoma vaccine)
www.dzhk.de – Deutsches Zentrum für Hirntumorenforschung
www.dmsg.de – Patienteninformationen zu Immuntherapien
📚 Wichtige Literatur
Liau LM et al., JAMA Oncol. 2023 (DCVax-L Phase 3 Trial)
Hilf N et al., Nature 2023 (NOA-16 RNA-Vaccine Study)
Keskin DB et al., Nature 2021 (Personalized Neoantigen Vaccines)
Wick W et al., Neuro-Oncology Practice 2022 (Review of Immunotherapy in GBM)
Reardon DA et al., Front Oncol. 2024 (Immunotherapy Landscape in Glioblastoma)
Zusammenfassung
Impftherapien beim Glioblastom sind ein aufstrebender, hochindividualisierter Therapieansatz.
Sie aktivieren gezielt das Immunsystem gegen Tumorzellen und zeigen in ersten Studien vielversprechende, aber noch experimentelle Ergebnisse.
Derzeit können Patient:innen nur im Rahmen klinischer Studien oder individueller Heilversuche teilnehmen.
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Informationen zum Themenkomplex
Dexamethason in der Neuroonkologie
Patienteninformation – Dexamethason in der Neuroonkologie?´
Dexamethason ist eines der am häufigsten eingesetzten Medikamente in der Neuroonkologie. Es hilft, Hirnschwellungen (Ödeme) zu reduzieren, die durch Tumoren, Operationen oder Bestrahlung entstehen können – und lindert damit Symptome wie Kopfschmerzen, Übelkeit oder neurologische Ausfälle.
Unsere Broschüre erklärt verständlich und fundiert,
wann und warum Kortikosteroide eingesetzt werden,
wie sie im Körper wirken,
welche Nebenwirkungen auftreten können – und wie man sie vermeiden oder abmildern kann.
Darüber hinaus werden aktuelle Studien, Dosierungsstrategien und mögliche Alternativen wie
Bevacizumab (Avastin®) – ein antiangiogenes Medikament, das Ödeme verringern kann, und
Boswellia serrata (Weihrauch-Extrakt) – eine pflanzliche, entzündungshemmende Option mit klinischer Evidenz,
übersichtlich vorgestellt.
Die Informationen richten sich an Patient:innen, Angehörige und behandelnde Ärzt:innen, die den Einsatz von Dexamethason besser verstehen und sicher begleiten möchten.
📄 Evidenzbasiert, praxisnah und aktuell – Stand: Oktober 2025
Mehr erfahren oder Broschüre herunterladen:
👉 Patienteninformation Dexamethason in der Neuroonkologie
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Informationen zum Themenkomplex
Vorasidenib bei niedriggradigen Gliomen ("lower grade gliomes")
Was ist Voranigo® (Vorasidenib)?
Voranigo® ist ein gezielt wirkendes, modernes Medikament zur Behandlung von IDH1- oder IDH2-mutierten Gliomen WHO-Grad 2 (Astrozytom oder Oligodendrogliom).
Die Therapie kommt nach der Operation zum Einsatz, wenn keine sofortige Strahlen- oder Chemotherapie erforderlich ist.
Es handelt sich um eine Tablettentherapie, die einmal täglich eingenommen wird und gezielt in den Stoffwechsel der Tumorzellen eingreift.
Wie funktioniert die Therapie?
Die meisten niedriggradigen Gliome tragen eine Mutation im Enzym IDH1 oder IDH2.
Diese Mutation führt zur Überproduktion eines „Onkometaboliten“ namens 2-Hydroxyglutarat (2-HG).
Dieser Stoff:
stört die epigenetische Regulation der Zelle (DNA- und Histon-Methylierung)
blockiert die normale Zelldifferenzierung
fördert das Tumorwachstum
Voranigo® hemmt selektiv die mutierten IDH1/IDH2-Enzyme.
Die Folgen:
2-HG sinkt deutlich,
Tumorzellen „beruhigen“ sich,
die Zellteilung verlangsamt sich,
das Fortschreiten des Tumors wird deutlich verzögert.
Vorasidenib wirkt gezielt auf den Ursprung der Erkrankung, ohne klassische Nebenwirkungen wie Haarausfall, Übelkeit oder Blutbildveränderungen, wie sie von Chemotherapien bekannt sind.
Wie wird Voranigo® eingenommen?
40 mg einmal täglich
Die Tablette wird nüchtern eingenommen
mindestens 2 Stunden vor der Einnahme nichts essen
mindestens 1 Stunde nach der Einnahme nichts essen
Tabletten nicht teilen, kauen oder zerdrücken
Wenn eine Dosis vergessen wurde:
→ innerhalb von 6 Stunden nachholen.
→ danach normal weiter.
Welche Vorteile bietet Voranigo®?
Die Wirksamkeit wurde in der großen INDIGO-Studie (Phase III, 331 Patient:innen) nachgewiesen.
Zentrale Ergebnisse:
Progressionsfreies Überleben (PFS):
Voranigo®: 27,7 Monate
Placebo: 11,1 Monate
Hazard Ratio: 0,39
→ entspricht einer 61 % Risikoreduktion für Tumorprogress.
Zeit bis zur nächsten Krebstherapie (Chemo oder Bestrahlung):
deutlich verlängert.
Die Therapie gilt als neuer Standard für Patient:innen mit IDH-mutiertem Gliom Grad 2.
Alltag mit Voranigo® – was ist wichtig?
Regelmäßige Kontrollen
Da Voranigo® die Leber belasten kann, sind Kontrollen nötig:
vor Beginn
alle 2 Wochen für 2 Monate
dann monatlich für 2 Jahre
danach nach Bedarf
Vermeiden von Wechselwirkungen
Nicht gemeinsam einnehmen mit:
starken CYP1A2-Hemmern (z. B. Ciprofloxacin, Fluvoxamin)
bestimmten Antiepileptika oder Immunsuppressiva
hormonellen Verhütungsmitteln (→ zusätzliche Barrieremethode notwendig)
Schwangerschaft & Stillzeit
→ kontraindiziert (embryotoxisch in Tierstudien).
→ Verhütung während der Behandlung + 2 Monate danach.
Nebenwirkungen
Voranigo® ist insgesamt gut verträglich.
Die häufigsten Nebenwirkungen sind:
Erhöhung der Leberwerte (ALT/AST)
Müdigkeit
Durchfall
Bauchschmerzen
leichte Thrombozytopenie
Lokale oder systemische schwere Nebenwirkungen sind selten.
Bei deutlichen Leberwerterhöhungen kann eine Dosisreduktion oder Pause notwendig sein.
Für wen ist Voranigo® geeignet?
Erwachsene (und Jugendliche ab 12 Jahren, ≥ 40 kg)
IDH1-R132- oder IDH2-R172-mutiertes Astrozytom/Oligodendrogliom
Nach Operation
Keine unmittelbare Notwendigkeit für Bestrahlung oder Chemotherapie
Gute Allgemeinverfassung (KPS meist ≥ 70)
Die Entscheidung erfolgt idealerweise im Molekularen Tumorboard.
Wissenschaftliche Literatur & medizinische Quellen
Klinische Wirksamkeit & Studien
Mellinghoff IK et al. Vorasidenib in IDH-mutant low-grade glioma (INDIGO). NEJM, 2023.
de la Fuente MI et al. Role of IDH inhibitors in gliomas. Neuro-Oncology, 2024.
Mechanismus & Präklinik
Konteatis Z et al. Vorasidenib: dual brain-penetrant IDH inhibitor. ACS Med Chem Lett, 2020.
Rudà R et al. IDH-mutant gliomas – biology and treatment. Nat Rev Neurol, 2024.
Offizielle Fachinformationen
EMA Produktinformation (2025)
Swissmedic Kurzbericht (2025)
Zusammenfassung
Voranigo® ist ein neues, zielgerichtetes Medikament, das speziell für Patient:innen mit IDH-mutierten Gliomen Grad 2 entwickelt wurde.
Es verlangsamt das Tumorwachstum,
verlängert die therapiefreie Zeit,
ist gut verträglich
und etabliert sich als neuer Standard in der neuroonkologischen Behandlung.
Weiterführende Informationen für Interessierte
Beispiele für bekannte, wichtige aber auch kontroverse Studien
🧠 Ausgewählte und kontrovers diskutierte Studien in der Neuroonkologie (Stand 2025)
Warum kontrovers? Teils wegen Studiendesign (z. B. fehlende Verblindung), mangelnder Replizierbarkeit, ethischer Fragen, Kosten/Nutzen oder Diskrepanzen zwischen Studienergebnissen und klinischer Praxis.
1) EF-14 (Tumor Treating Fields – TTFields beim Glioblastom)
Publikation: Stupp et al., JAMA 2017
Design: Phase-III, TTFields + Temozolomid vs. Temozolomid allein (ndGBM).
Kontroverse: Längeres medianes OS (20,9 vs. 16,0 Monate), aber keine Verblindung, begrenzte externe Validität, unklare Wirkhypothese und sehr hohe Kosten (> 20 000 €/Monat).
Diskussion: In Europa zurückhaltende Nutzung, in den USA breite Implementierung. Stand 2025: Bestandteil der Regeltherapie bei ndGBM und ZNS-WHO-Grad-4-Astrozytom; Adhärenz im Alltag bleibt variabel.
2) CheckMate 498 & 548 (Nivolumab beim Glioblastom)
Publikationen: Lim et al., Neuro-Oncology 2022; Omuro et al., Neuro-Oncology 2023
Design: Phase-III PD-1-Blockade bei ndGBM (MGMT-methyliert bzw. -unmethyliert).
Kontroverse: Kein OS-Vorteil.
Diskussion: Checkpoint-Inhibition bleibt bei „kalten“ Tumoren wie GBM weitgehend ineffektiv; trotz hoher Patientenerwartung weiterhin experimentell (auch prä-/neoadjuvant).
3) NOA-16 (IDH1-Peptid-Vakzine bei Astrozytom WHO 2/3)
Publikation: Platten et al., Nature 2021
Design: Phase I/II – Sicherheit und Immunogenität einer IDH1(R132H)-Vakzine.
Kontroverse: Starke Immunantworten, aber keine prospektiv belegte Überlebensverbesserung; mediale Euphorie → Übererwartungen.
Diskussion: Wichtiges „Proof-of-Principle“, klinisch noch nicht standardreif.
4) CODEL vs. CATNON (Therapiestrategien bei IDH-mut. WHO-Grad-3-Gliomen)
Publikationen: CATNON: van den Bent et al., NEJM 2017; CODEL: laufend
Design: PCV vs. Temozolomid in IDH-mutierten Anaplastika.
Kontroverse: CATNON zeigte TMZ-Nutzen, ohne IDH-Stratifizierung; CODEL stellt TMZ-Rolle zugunsten PCV in Frage.
Diskussion: Uneinheitliche Standards zwischen Leitlinien und Zentren; starke Praxis-Heterogenität.
5) Deutsches Gliomnetzwerk – MGMT-Promotor-Methylierung
Publikationen: z. B. Weller et al., JCO 2015
Design: Prädiktiver Marker für TMZ-Wirksamkeit.
Kontroverse: Inter-Labor-Variabilität, fehlende einheitliche Cut-offs.
Diskussion: Prädiktiv vs. prognostisch? Klinisches Dilemma bei „borderline MGMT“.
6) Personalisierte Neoantigen-Peptidimpfung (Real-World, 2015–2023)
Publikation: Latzer et al., Nature Communications 2024
Design: Retrospektive Real-World-Analyse, n = 173 GBM-Patient:innen mit personalisierter Peptidvakzine.
Ergebnisse: Median-OS 31,9 Monate; 90 % zeigten Vakzin-induzierte T-Zell-Antworten; Responder mit medianem OS 53 Monate vs. 27 Monate bei Non-Respondern; niedrige Toxizität.
Kontroverse: Nicht-randomisiert, Selbstselektion/-finanzierung, potenzielle Survivor-Bias, nur propensity-gematchte historische Vergleiche.
Diskussion: Technisch machbar und immunologisch vielversprechend, aber Bestätigung durch randomisierte Studien erforderlich.
7) ACT IV (Rindopepimut – EGFRvIII-Vakzine beim Glioblastom)
Publikation: Weller et al., Lancet Oncology 2017
Design: Phase-III, doppelblind, EGFRvIII-Vakzine + Standard vs. Placebo.
Kontroverse: Vorzeitig wegen Futility beendet; kein OS-Benefit.
Diskussion: EGFRvIII-Antigenverlust und Tumorheterogenität als Schlüsselhürden für Vakzinstrategien.
8) BELOB / EORTC 26101 (Bevacizumab bei rGBM)
Publikationen: Taal et al., Lancet Oncol. 2014; Wick et al., Lancet Oncol. 2017
Design: Bevacizumab ± Lomustin beim Rezidiv.
Kontroverse: PFS-Gewinn ohne OS-Vorteil.
Diskussion: Weiterhin genutzt zur Symptomkontrolle (Ödem, Steroid-Sparing), aber nicht krankheitsmodifizierend; Kosten-/Nutzen-Debatte.
9) GAPVAC-101 (Aktiv personalisierte Vakzine bei ndGBM)
Publikation: Hilf et al., Nature 2019
Design: Phase I, multipeptid-personalisiert nach Radiochemotherapie.
Ergebnisse: Produktion binnen ~12 Wochen machbar; breite T-Zell-Antworten; PFS 14,2 Mon., OS 29 Mon.
Diskussion: Wegweisendes Konzept, aber komplex/teuer; bislang frühe Evidenz.
10) H3K27M-Vakzine bei diffusem Mittelliniengliom (Erwachsene)
Publikation: Grassl et al., Nature Medicine 2023
Design: Compassionate-Use-Serie (n = 8).
Ergebnisse: Starke T-Zell-Antworten, frühe klinische Signale.
Kontroverse: Kleine, heterogene Kohorte, keine Kontrolle.
Diskussion: Ermutigend für pädiatrie-ähnliche Mittelliniengliome; Bedarf an prospektiven Studien.
Fazit (2025)
Richtung individualisierte Immuntherapien ist klar, harte klinische Endpunkte fehlen jedoch oft.
Zentrale Hürden: Biomarker-Selektion, Tumorheterogenität, robuste Studiendesigns und Machbarkeit/Kosten.
Konsens: Wir brauchen randomisierte, biomarkergesteuerte Multicenter-Studien und internationale Kooperation, um von „Signalen“ zu neuen Standards zu kommen.
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Erstdiagnose
Glioblastom
Broschüre „Glioblastom – verständlich erklärt“
Kompakter, aktueller Überblick: Von der Diagnose über Operation, Bestrahlung, Chemotherapie bis zur Nachsorge – fachlich fundiert und leicht verständlich aufbereitet.
Ideal für Patienten, Angehörige & Interessierte.
(Weiterleitung an externe Website, payhip):
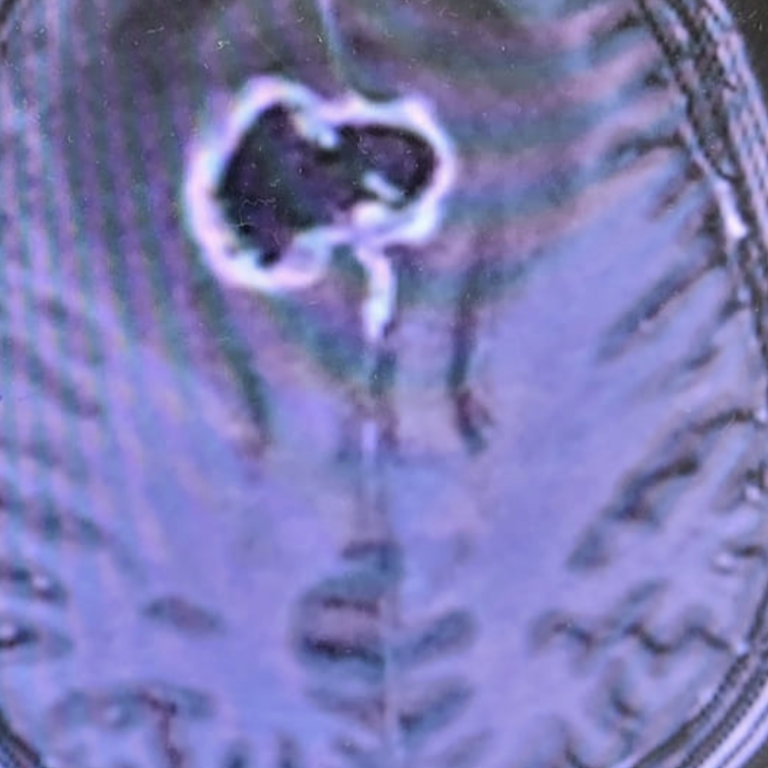
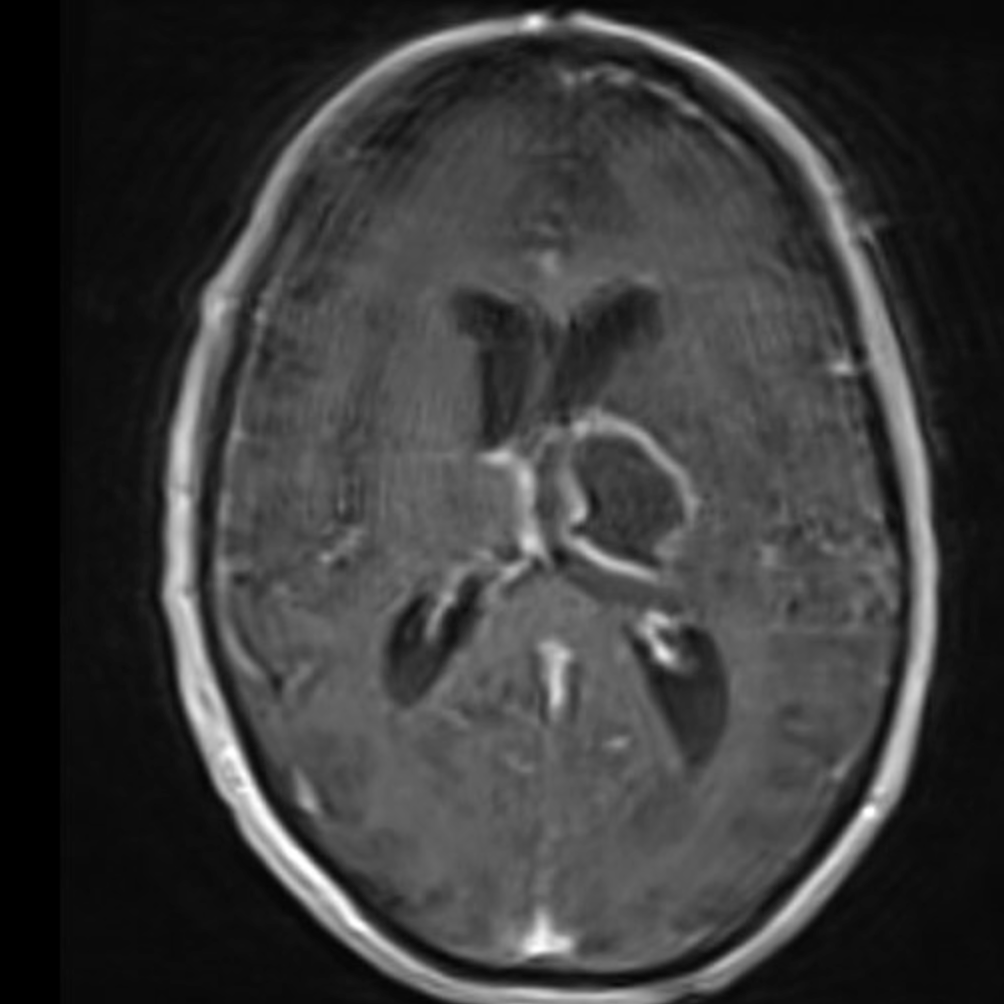
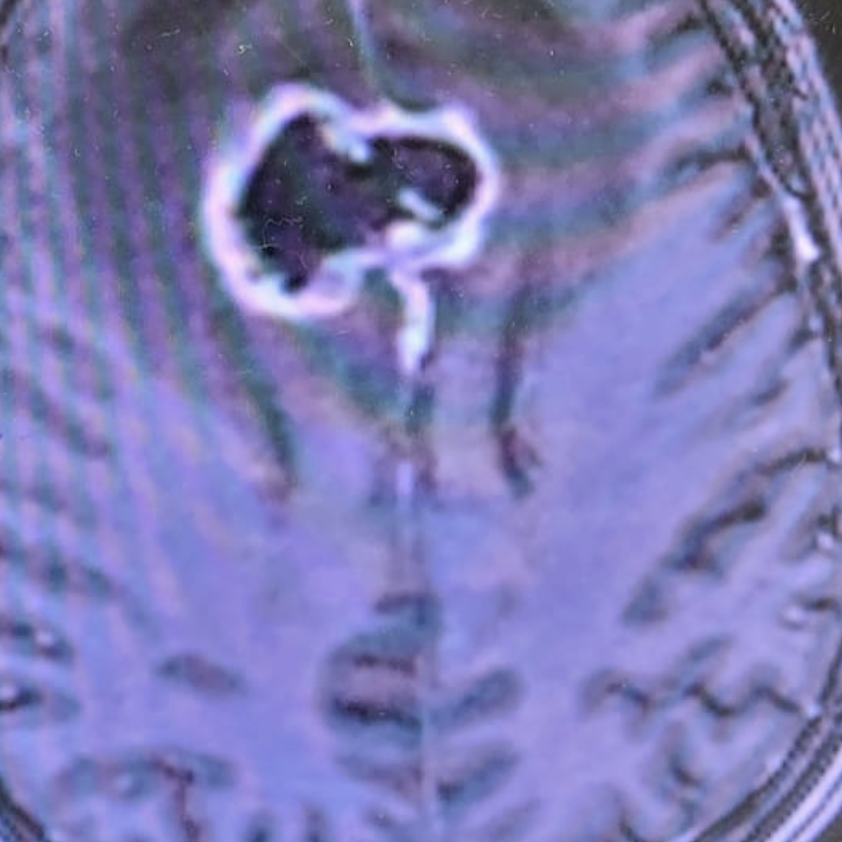
Kontrastmittel aufnehmende Raumforderung (sog. Balkengliom) in einem axial geschichteten T1-KM MRT des Neurokraniums (cMRT).
Die das Verhalten einer Raumforderung im Schädelkinneren im KM-MRT (Kontrastmittel-MRT) kann oft schon entscheidende Informationen liefern über die wahrscheinliche Art des Tumors. Das ersetzt nach aktuellem Wissensstand jedoch keine feingewebliche Untersuchung!
Antragsvorlagen für individuelle Heilversuche
Stand 15.10.2025
Individueller Heilversuch mit Bevacizumab (Avastin®) bei Radionekrose
Diese Vorlage unterstützt bei der Beantragung einer Bevacizumab-Therapie bei Strahlennekrose nach Glioblastom- oder Hirnmetastasenbehandlung.
Beinhaltet vollständigen Antragstext, aktuelle Evidenz (z. B. Neuro-Oncology Advances 2022) und Platzhalter für Patientendaten, Verlauf und Bildgebung.
Vorlage zum Erwerben (Weiterleitung an externe Website, payhip):
Individueller Heilversuch mit Regorafenib (Stivarga®) bei Rezidiv-Glioblastom
Professionelle Word-Vorlage für Off-Label-Anträge bei therapierefraktärem Glioblastom (ab abgeschlosseneer Erstlinien-Therapie).
Basierend auf der REGOMA-Studie (JCO 2019) und Real-World-Analysen (Lombardi 2024).
Strukturiert nach klinischem Verlauf, Molekularbefunden und aktueller Evidenz.
Vorlage zum Erwerben (Weiterleitung an externe Website, payhip):
Individueller Heilversuch mit Pembrolizumab (Keytruda®)
Vorlage zur Beantragung einer Immuncheckpoint-Blockade bei fortgeschrittenen oder therapierefraktären ZNS-Tumoren, insbesondere: Glioblastom IDH-WT mit hoher PD-L1-Expression, Mismatch-Repair-defiziente (MMR-def.) oder MSI-high Tumoren, oder bei Patienten mit Hirnmetastasen solider Tumoren (z. B. NSCLC, Melanom) nach Ausschöpfung der Standardtherapien.
Die Vorlage enthält juristisch korrekte Formulierungen, die aktuelle Studienlage (JCO 2023, Neuro-Oncology 2024) sowie Hinweise zur Patientenselektion nach Biomarkern (PD-L1, MMR-Status, TMB).
Vorlage zum Erwerben (Weiterleitung an externe Website, payhip):
Vorlage noch in Bearbeitung
Individueller Heilversuch mit Encorafenib (Braftovi®)
Antragsvorlage zur Beantragung einer zielgerichteten Therapie bei BRAF-V600E-mutierten Gliomen oder Hirnmetastasen (z. B. Melanom, NSCLC, kolorektales Karzinom). Beruht auf der aktuellen Evidenzlage aus Neuro-Oncology 2022 und JAMA Oncol 2023, die die Wirksamkeit der BRAF-/MEK-Inhibition im ZNS-Kontext belegt. Strukturiert, evidenzbasiert und klinisch relevant für personalisierte neuroonkologische Therapiekonzepte.
Ideal für den Antrag beim Kostenträger nach Ausschöpfung aller leitliniengerechten Optionen.
Vorlage zum Erwerben (Weiterleitung an externe Website, payhip):
Vorlage noch in Bearbeitung
Antragsvorlagen
Nutzen Sie unsere praxisnahen Vorlagen für Ihre individuellen Antragsstellungen.
Aktuelle Literatur
Lesen Sie die neuesten Entwicklungen und Studien im Bereich Neuroonkologie.
Compassionate Use Programme (Härtefallprogramme)
Definition und Grundlagen
´Compassionate Use Programme (Härtefallprogramme)
Was ist ein Compassionate Use Programm (CUP)?
Ein Compassionate Use Programm (deutsch: Härtefallprogramm) ermöglicht Patientinnen und Patienten den Zugang zu noch nicht zugelassenen Arzneimitteln, wenn keine alternative, zugelassene Therapie mehr zur Verfügung steht und ein begründeter wissenschaftlicher Therapieansatz besteht.
Diese Programme dienen dazu, Patient:innen mit schweren, lebensbedrohlichen oder seltenen Erkrankungen frühzeitig Zugang zu potenziell wirksamen neuen Therapien zu verschaffen.
In Deutschland sind Compassionate Use Programme in § 80 des Arzneimittelgesetzes (AMG) sowie in der Arzneimittel-Härtefall-Verordnung (AMHV) geregelt.
Die zuständige Behörde ist das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM).
Rechtliche Grundlage (§ 80 AMG, § 2 AMHV)
Ein Compassionate Use Programm kann nur beantragt werden, wenn:
Eine schwerwiegende, lebensbedrohliche oder seltene Erkrankung vorliegt.
Keine zugelassene Therapieoption verfügbar ist oder ausgeschöpft wurde.
Das betreffende Arzneimittel mindestens in einem fortgeschrittenen Entwicklungsstadium ist (z. B. Phase III oder Zulassungsantrag eingereicht).
Ein wissenschaftlich begründeter Nutzen zu erwarten ist, basierend auf klinischen Daten.
Das Programm wird durch den pharmazeutischen Unternehmer beim BfArM angezeigt und von dort geprüft und bestätigt.
Eine Liste aller aktuell laufenden Compassionate Use Programme ist auf der offiziellen BfArM-Website abrufbar:
www.bfarm.de → Arzneimittel → Compassionate Use
Ablauf und Beteiligte
Anzeige durch den Hersteller:
Das Pharmaunternehmen beantragt beim BfArM die Genehmigung für ein Härtefallprogramm für eine definierte Patientengruppe.
Bestätigung durch das BfArM:
Nach positiver Prüfung wird das Programm veröffentlicht und kann durch Ärzt:innen genutzt werden.
Behandelnde Ärztin / behandelnder Arzt:
Stellt fest, dass Patient:innen die Einschlusskriterien erfüllen, und beantragt individuell die Aufnahme in das Programm.
Kostenübernahme:
Die Bereitstellung des Medikaments erfolgt kostenfrei durch den Hersteller; es handelt sich nicht um eine GKV-Leistung.
Dokumentation und Meldung:
Ärzt:innen müssen die Anwendung und etwaige Nebenwirkungen dokumentieren und dem pharmazeutischen Unternehmer melden.
Ethische und klinische Bedeutung
Compassionate Use Programme sind ein wichtiges Bindeglied zwischen klinischer Forschung und Versorgung.
Sie ermöglichen Patient:innen Zugang zu innovativen Therapien – oft Monate vor einer Zulassung – und erlauben gleichzeitig die Beobachtung des Sicherheitsprofils unter realen Bedingungen.
Gerade in der Neuroonkologie (z. B. bei diffusen Gliomen, Hirnstammgliomen oder LMD) bieten sie oft die einzige Option, neue Substanzen mit vielversprechenden Mechanismen anzuwenden.
Hinweis
Compassionate Use Programme unterliegen der ärztlichen Schweigepflicht und dem Datenschutz nach DSGVO.
Sie ersetzen keine zugelassene Therapie, sondern bieten eine begrenzte, regulierte Option, wenn medizinisch vertretbar und im Sinne des Patientenwohls.
Informationen zu laufenden Programmen finden Sie auf der Website des BfArM oder über den jeweiligen pharmazeutischen Hersteller.
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.
Übersicht relevanter Literatur
Individuelle Heilversuche und Tumorboards
Literaturübersicht – Individuelle Heilversuche, Präzisionsonkologie & Neuroonkologie (Stand: Oktober 2025)
Gladstone BP, Beha J, Hakariya A, et al. Systematic review and meta-analysis of molecular tumor board data on clinical effectiveness and evaluation gaps. npj Precision Oncology. 2025;9:96.
https://doi.org/10.1038/s41698-025-00863-3
Herrero Colomina J, Johnston E, Duffus K, et al. Real-world experience of Molecular Tumour Boards for clinical decision-making for cancer patients. npj Precision Oncology. 2025;9:87.
https://doi.org/10.1038/s41698-025-00863-3
Huang B, Edwards J, et al. Molecular Tumor Board Review and Improved Overall Survival: A Case-Control Study. JCO Precision Oncology. 2021;5:1331–1342.
https://pubmed.ncbi.nlm.nih.gov/34622117
Zarkavelis G, Giannoulatou E, Tzogani K, et al. Off-label despite high-level evidence: a clinical practice review of commonly used off-patent cancer medicines. ESMO Open. 2023;8(1):100604.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10024100
Boos L, Wicki A. The molecular tumor board — a key element of precision oncology. memo – Magazine of European Medical Oncology. 2024;17:190–193.
https://doi.org/10.1007/s12254-024-00977-7
Faust A, et al. Should the governance of individual treatment attempts (ITAs) be regulated? medRxiv preprint. 2022.
https://doi.org/10.1101/2022.03.21.22272689
Vollmann J, Schildmann J. Off-label use, compassionate use und individuelle Heilversuche: ethische Implikationen zulassungsüberschreitender Arzneimittelanwendungen. Ethik in der Medizin. 2023;35(2):145–155.
https://doi.org/10.1007/s00481-023-00627-8
Le Rhun E, Bink A, Felsberg J, et al. The clinical and molecular landscape of diffuse hemispheric glioma, H3 G34-mutant. Neuro-Oncology. 2025;27(6):1519–1535.
https://doi.org/10.1093/neuonc/noaf015
Patel A, Göbel K, Ille S, et al. Prospective, multicenter validation of a platform for rapid molecular profiling of central nervous system tumors. Nature Medicine. 2025;31(5):1567–1577.
https://doi.org/10.1038/s41591-025-03562-5
Nozzoli F, Rahmanzade R, Schmid S, et al. Distinct molecular profile and outcome of oligodendroglioma, IDH-mutant, 1p/19q-codeleted and TERTp-wildtype. Neuro-Oncology. 2025;doi:10.1093/neuonc/noaf141.
https://doi.org/10.1093/neuonc/noaf141
Wen PY, Weller M, Lee EQ, et al. Glioblastoma in Adults: A Society for Neuro-Oncology (SNO) and European Society of Neuro-Oncology (EANO) Consensus Review on Current Management and Future Directions. Neuro-Oncology. 2025;doi:10.1093/neuonc/noaf177.
https://doi.org/10.1093/neuonc/noaf177
Wick W, Lanz L-M, Wick A, et al. Molecularly matched targeted therapies plus radiotherapy in glioblastoma: the phase 1/2a N2M2 umbrella trial. Nature Medicine. 2025;doi:10.1038/s41591-025-03928-9.
https://doi.org/10.1038/s41591-025-03928-9
Wick W, et al. EANO guidelines on the diagnosis and treatment of adult gliomas: 2024 update. Neuro-Oncology. 2024;26(Suppl 2):ii1–ii48.
https://doi.org/10.1093/neuonc/noae020
Schmid AC, et al. Off-label targeted therapies in neuro-oncology: challenges and opportunities. Current Opinion in Neurology. 2023;36(6):667–676.
https://doi.org/10.1097/WCO.0000000000001238
Duvivier HL, et al. Pembrolizumab in patients with tumors with high tumor mutational burden: results from the TAPUR study. Journal of Clinical Oncology. 2023;41(33):5140–5150.
https://doi.org/10.1200/JCO.23.00702
Hinweis:
Die auf dieser Seite bereitgestellten Informationen und Dokumente dienen ausschließlich der allgemeinen wissenschaftlichen und ärztlichen Orientierung im Bereich der Neuroonkologie und individueller Heilversuche. Sie stellen keine ärztliche Beratung, Diagnose oder Therapieempfehlung dar und ersetzen keinesfalls die individuelle klinische Beurteilung oder Entscheidung der behandelnden Ärztinnen und Ärzte.
Alle Inhalte wurden mit größtmöglicher Sorgfalt erstellt, können jedoch Fehler oder Unvollständigkeiten enthalten. Eine Haftung für die Richtigkeit, Vollständigkeit oder Aktualität der bereitgestellten Informationen wird nicht übernommen.
Die Nutzung der Inhalte erfolgt auf eigene Verantwortung. Entscheidungen zu Diagnostik oder Therapie sind stets unter Berücksichtigung der aktuellen Leitlinien, Fachinformationen und individuellen Patientensituation zu treffen.
© 2025. Alle Rechte vorbehalten. Jede Vervielfältigung, Weitergabe oder kommerzielle Nutzung der Vorlagen, Texte oder Dokumente ist ohne schriftliche Genehmigung untersagt.